A aplicação imunoistoquímica do anticorpo
anti-Bcl2 (clone 124, o mais usado) é, na maior parte das vezes, útil e suficiente no diagnóstico do
Linfoma Folicular. Sua positividade nos centros germinativos é muito
contrastante com casos de hiperplasia folicular reacional que são sempre
Bcl2 negativos. Entretanto, são descritos casos de Linfoma Folicular
Bcl2-negativos (ao menos 10% dos casos) e o motivo da tal negatividade para o imunomarcador Bcl2 pode ser
atribuído (a) à sensibilidade do clone 124; (b) a ausência do rearranjo
t(14;18), característico da neoplasia.
Há clones diferentes para imunomarcadores semelhantes. Na hematoncologia é bem conhecida a baixa sensibilidade de marcadores fabricados anteriormente ao SP4 para a reação da Ciclina-D1 no diagnóstico do Linfoma do Manto. A possibilidade de falso-negativo do clone 124 no Linfoma Folicular, entretanto, é menos comentada e essa possibilidade pode ser contornada em alguns casos com a utilização complementar do clone E17. Nos casos tanto 124 e E17 negativos, o raciocínio retorna para a questão da translocação t(14;18).
O gene que codifica a proteína Bcl2 é um oncogene (logo, existe normalmente) e possui uma função anti-apoptótica (contrabalanceada pelo gene BAX, da mesma família). O Bcl2 regula negativamente a apoptose e, em sua função normal, impede que células entrem em morte programada (é normalmente negativo, portanto, em centros terminativos reacionais). Sua alteração genética ocorre justapondo o gene BCL2 ao gene que produz a cadeia pesada das imunoglobulinas (@IGH). A alteração além de resultar em hiperexpressão da proteína nas células (detectável pela imunoistoquímica), também concede vantagem proliferativa aos clones de linfócitos mutados. Nesse ponto, vale lembrar que linfomas agressivos ditos double-hit apresentam como opção de segunda alteração gênica a mutação do BLC2 e, portanto, com características antiapoptóticas além da vantagem proliferativa concedida pela primeira mutação (no locus MYC/8q24).
A translocação t(14;18) é a principal alteração relacionada à hiperexpressão do Bcl2. Entretanto, observam-se linfomas foliculares que não apresentam tal translocação e a etiopatogênese nestes casos não pode ser explicada com outros argumentos. Mais importante na prática do patologista, o diagnóstico nestes casos torna-se muito difícil e irá se balizar na morfologia dos agregados linfoides e na exclusão de outros linfomas. Vale aqui também lembrar que os linfomas foliculares primários da pele (ditos centrofoliculares) diversamente, são, na maior parte, Bcl-2 negativos e não mostram a t(14;18).
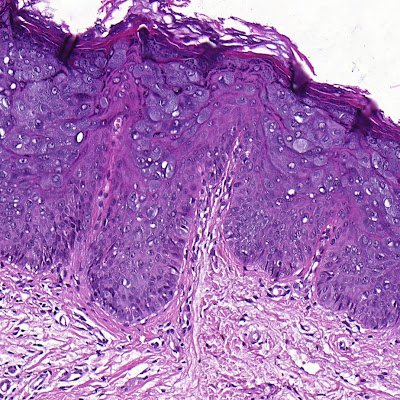
As fotos abaixam ilustram um caso de linfoma folicular do mediastino recidivado de um paciente adulto. O Bcl2 foi negativo nos dois clones testados (124 e E17) e o teste do rearranjo t(14;18) também foi negativo. O diagnóstico se baseia neste caso na morfologia: arquitetura folicular e células polimorfas (bifenotípicas: ora centroblásticas e ora centróciticas). O CD23 mostra positividade para células além daquelas normalmente positivas nos centros germinativos e também a co-expressão de CD5. O MUM1 foi positiva em subset de linfócitos (vide comentários sobre este marcador em posts posteriores).
Há clones diferentes para imunomarcadores semelhantes. Na hematoncologia é bem conhecida a baixa sensibilidade de marcadores fabricados anteriormente ao SP4 para a reação da Ciclina-D1 no diagnóstico do Linfoma do Manto. A possibilidade de falso-negativo do clone 124 no Linfoma Folicular, entretanto, é menos comentada e essa possibilidade pode ser contornada em alguns casos com a utilização complementar do clone E17. Nos casos tanto 124 e E17 negativos, o raciocínio retorna para a questão da translocação t(14;18).
O gene que codifica a proteína Bcl2 é um oncogene (logo, existe normalmente) e possui uma função anti-apoptótica (contrabalanceada pelo gene BAX, da mesma família). O Bcl2 regula negativamente a apoptose e, em sua função normal, impede que células entrem em morte programada (é normalmente negativo, portanto, em centros terminativos reacionais). Sua alteração genética ocorre justapondo o gene BCL2 ao gene que produz a cadeia pesada das imunoglobulinas (@IGH). A alteração além de resultar em hiperexpressão da proteína nas células (detectável pela imunoistoquímica), também concede vantagem proliferativa aos clones de linfócitos mutados. Nesse ponto, vale lembrar que linfomas agressivos ditos double-hit apresentam como opção de segunda alteração gênica a mutação do BLC2 e, portanto, com características antiapoptóticas além da vantagem proliferativa concedida pela primeira mutação (no locus MYC/8q24).
A translocação t(14;18) é a principal alteração relacionada à hiperexpressão do Bcl2. Entretanto, observam-se linfomas foliculares que não apresentam tal translocação e a etiopatogênese nestes casos não pode ser explicada com outros argumentos. Mais importante na prática do patologista, o diagnóstico nestes casos torna-se muito difícil e irá se balizar na morfologia dos agregados linfoides e na exclusão de outros linfomas. Vale aqui também lembrar que os linfomas foliculares primários da pele (ditos centrofoliculares) diversamente, são, na maior parte, Bcl-2 negativos e não mostram a t(14;18).
As fotos abaixam ilustram um caso de linfoma folicular do mediastino recidivado de um paciente adulto. O Bcl2 foi negativo nos dois clones testados (124 e E17) e o teste do rearranjo t(14;18) também foi negativo. O diagnóstico se baseia neste caso na morfologia: arquitetura folicular e células polimorfas (bifenotípicas: ora centroblásticas e ora centróciticas). O CD23 mostra positividade para células além daquelas normalmente positivas nos centros germinativos e também a co-expressão de CD5. O MUM1 foi positiva em subset de linfócitos (vide comentários sobre este marcador em posts posteriores).
Células polimorfas (bifenotípicas: ora centroblásticas e ora centróciticas). Como há uma predominância de centroblastos (concordam?) acho que cabe aqui a classificação 3a da OMS 2008.
CD10+ (vide o mesmo filete nervoso que é demonstrado na foto do HE com algumas células fortemente CD10+). Vejam que a reação do CD10 em linfócitos é quase sempre meio que "desmaiada"(fraca).
CD23 positivo tanto na trama do centro germinativo quanto em células fora desse contexto/localização (vide o mesmo filete nervoso que é demonstrado na foto do HE)
Detalhe de outra positividade do CD23
Positividade do CD5 (interessante no Linfoma Folicular - será discutida em outro post)
Positividade para Bcl6 (vide o mesmo filete nervoso que é demonstrado na foto do HE)
PS: 1- Esse caso também foi positivo (em algumas células) para o MUM.1 e tal expressão também será discutida em outro post (porque agora eu vou dormir). Abraços, Fred. 2- Não hesitem em deixar algum comentário em casos de dúvida! 3- Se quiserem publicar alguma coisa aqui (eu ficaria feliz!) basta me mandar as fotos e o texto no meu email fhcmelo@gmail.com. Pelo menos tentem fazer alguma vez, é um ótimo exercício didático/de aprendizagem.